Essais cliniques : Avantages et risques pour les participants
Les essais cliniques constituent une étape cruciale dans le développement de nouveaux médicaments et traitements médicaux. Ces études scientifiques rigoureusement encadrées permettent d’évaluer l’efficacité et la sécurité des innovations thérapeutiques avant leur autorisation pour une utilisation plus large. Pour les patients et volontaires sains qui y participent, ces essais représentent à la fois une opportunité et un engagement qui mérite réflexion.
Chaque année en France, des milliers de personnes s’engagent dans des essais cliniques, contribuant ainsi directement à l’avancée de la médecine. Que vous souffriez d’une maladie pour laquelle les traitements actuels sont insuffisants ou que vous envisagiez une participation comme volontaire sain, comprendre les avantages potentiels et les risques associés est essentiel.
Cet article vous propose un panorama complet des essais cliniques, de leur organisation aux considérations pratiques pour les participants. Nous examinerons les bénéfices personnels et collectifs que peuvent apporter ces études, mais aussi les précautions à prendre et les questions à se poser avant de s’engager dans cette démarche.

Comprendre les essais cliniques
Un essai clinique est une recherche médicale menée sur des êtres humains pour évaluer l’efficacité et la sécurité d’une nouvelle approche thérapeutique. Ces études suivent une méthodologie scientifique rigoureuse et sont soumises à des règles éthiques strictes avant, pendant et après leur réalisation.
Types d’essais cliniques
Les essais cliniques peuvent varier selon leurs objectifs et méthodologies :
- Essais thérapeutiques : ils évaluent de nouveaux médicaments, dispositifs médicaux ou protocoles de soins
- Essais préventifs : ils étudient des stratégies pour prévenir l’apparition de maladies
- Essais diagnostiques : ils visent à améliorer la détection ou le diagnostic de pathologies
- Essais sur la qualité de vie : ils examinent comment améliorer le confort et le bien-être des patients
- Essais observationnels : ils observent les participants sans intervention spécifique, pour comprendre l’évolution naturelle d’une maladie ou les effets de traitements standards
Selon la méthodologie employée, on distingue également :
- Essais randomisés : les participants sont répartis au hasard entre différents groupes de traitement
- Essais en double aveugle : ni les participants ni les investigateurs ne savent qui reçoit le traitement étudié ou le placebo/traitement de référence
- Essais ouverts : tous les participants reçoivent le traitement à l’étude, sans groupe de comparaison
Phases d’un essai clinique
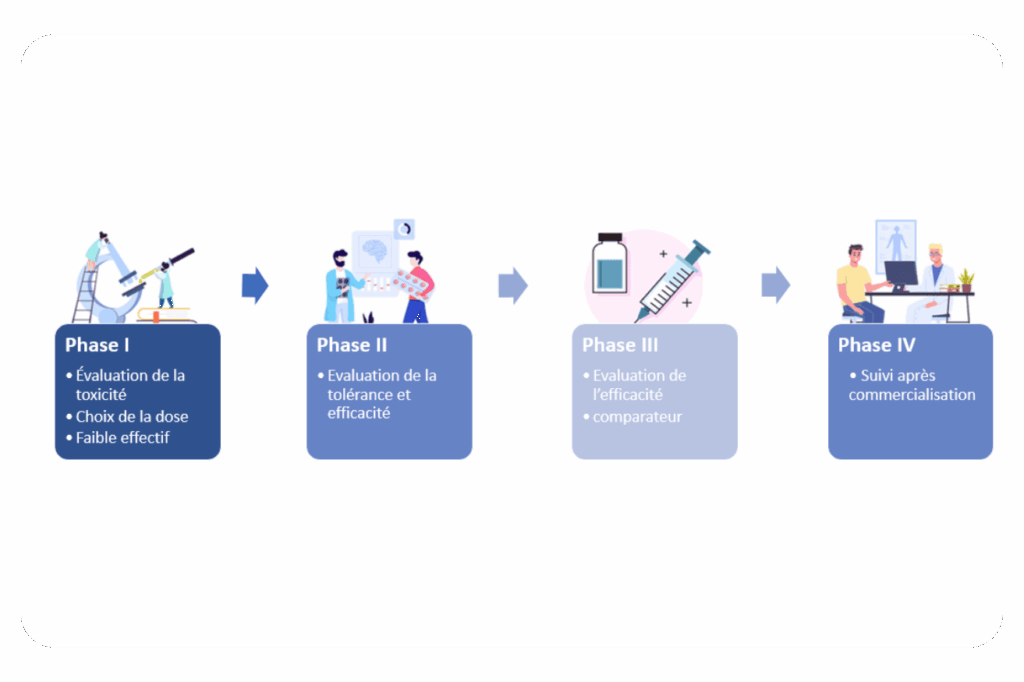
Le développement d’un nouveau traitement suit généralement un parcours en plusieurs phases, chacune ayant des objectifs spécifiques :
| Phase | Objectifs | Participants | Durée moyenne | Risques |
|---|---|---|---|---|
| Phase I | Évaluer la sécurité, déterminer le dosage sûr, observer les effets secondaires | 20 à 100 volontaires sains (parfois des patients) | Plusieurs mois | Potentiellement élevés (première utilisation chez l’humain) |
| Phase II | Évaluer l’efficacité et poursuivre l’étude de la sécurité | 100 à 500 patients atteints de la maladie ciblée | Plusieurs mois à 2 ans | Modérés à élevés |
| Phase III | Confirmer l’efficacité, surveiller les effets secondaires, comparer aux traitements standards | 1000 à 5000 patients | 1 à 4 ans | Mieux caractérisés mais toujours présents |
| Phase IV | Surveiller l’efficacité et la sécurité à long terme après commercialisation | Plusieurs milliers de patients | Années | Généralement plus faibles (médicament déjà autorisé) |
Cette progression méthodique permet d’accumuler des connaissances sur le traitement tout en limitant l’exposition aux risques pour les participants. En France, toutes ces phases sont supervisées par l’Agence Nationale de Sécurité du Médicament et des produits de santé (ANSM) ainsi que par des Comités de Protection des Personnes (CPP).
Avantages de la participation
La participation à un essai clinique peut présenter plusieurs bénéfices, tant pour les volontaires eux-mêmes que pour la société dans son ensemble. Ces avantages varient selon le type d’essai et la situation personnelle du participant.
Accès à des traitements innovants
L’un des principaux attraits des essais cliniques est la possibilité d’accéder à des traitements qui ne sont pas encore disponibles sur le marché :
- Pour les personnes atteintes de maladies graves ou rares, les essais peuvent représenter une option thérapeutique quand les traitements standards sont inefficaces ou inexistants
- Les traitements expérimentaux peuvent parfois offrir de meilleures perspectives que les thérapies conventionnelles
- Dans certains cas, les participants peuvent continuer à bénéficier du traitement après la fin de l’essai, si celui-ci s’est avéré efficace
L’INSERM rapporte que pour certaines pathologies comme les cancers avancés ou les maladies neurodégénératives, les essais cliniques constituent parfois la seule possibilité d’accès à des thérapies prometteuses. Toutefois, il est important de noter qu’il n’y a aucune garantie que le traitement à l’étude sera plus efficace que les traitements existants ou qu’un placebo.
Suivi médical renforcé
Les participants aux essais cliniques bénéficient généralement d’un suivi médical particulièrement attentif :
- Examens réguliers et approfondis, souvent plus fréquents que dans le cadre d’une prise en charge standard
- Équipe médicale spécialisée et disponible pour répondre aux questions et préoccupations
- Surveillance étroite de l’évolution de la maladie et des éventuels effets secondaires
- Accès à des tests et examens parfois coûteux ou peu disponibles en pratique courante
Ce suivi renforcé peut permettre une détection précoce de complications ou d’évolutions de la maladie, et contribue à la sécurité globale du participant. Tous les frais liés à l’essai sont généralement pris en charge intégralement, y compris les déplacements dans certains cas.
Quels sont les avantages de participer à un essai clinique ?
Participer à un essai clinique permet d’accéder à des traitements innovants avant leur commercialisation, de bénéficier d’un suivi médical renforcé avec des examens fréquents et spécialisés, et de contribuer à l’avancement de la recherche médicale. Les participants reçoivent souvent une information détaillée sur leur état de santé et leur maladie. Certains essais prévoient également une indemnisation pour le temps consacré et les contraintes subies.
Risques et considérations
La participation à un essai clinique comporte également des risques et inconvénients qu’il est essentiel d’évaluer soigneusement avant de s’engager. Ces considérations varient selon la nature de l’essai et le stade de développement du traitement étudié.
Effets secondaires potentiels
Les traitements expérimentaux peuvent entraîner des effets indésirables de gravité variable :
- Effets secondaires connus : déjà observés lors d’études précédentes ou avec des traitements similaires
- Effets secondaires inconnus : particulièrement dans les premières phases d’essai, tous les risques ne sont pas encore identifiés
- Interactions médicamenteuses : possibles réactions avec d’autres traitements que prend le participant
- Effets à long terme : certaines conséquences peuvent n’apparaître que tardivement, après la fin de l’essai
Selon l’ANSM, la survenue d’effets indésirables graves reste relativement rare grâce aux précautions prises dans la conception des essais et à la surveillance médicale. Néanmoins, en 2022, 479 effets indésirables graves liés à des recherches impliquant la personne humaine ont été déclarés en France, dont 17 ont entraîné le décès du participant.
Incertitudes liées aux nouveaux traitements
Participer à un essai clinique signifie accepter plusieurs formes d’incertitude :
- Efficacité non prouvée : le traitement peut s’avérer inefficace pour traiter la condition étudiée
- Possibilité de recevoir un placebo : dans les essais contrôlés, certains participants ne reçoivent pas le traitement actif
- Contraintes pratiques : visites fréquentes à l’hôpital, examens nombreux, restrictions alimentaires ou d’activité
- Impact sur la qualité de vie : certains protocoles peuvent être contraignants au quotidien
- Risque d’arrêt prématuré : l’essai peut être interrompu si des problèmes de sécurité surviennent
Il est crucial de comprendre que la participation à un essai clinique ne garantit pas un bénéfice personnel, même si elle contribue à l’avancement des connaissances médicales.
Points à considérer avant de participer
- Votre état de santé actuel et les alternatives thérapeutiques disponibles
- La phase de l’essai clinique (les essais de phase précoce comportent généralement plus de risques)
- La durée et les contraintes pratiques de l’essai
- Les effets secondaires potentiels et leur impact sur votre qualité de vie
- Votre compréhension des objectifs et de la méthodologie de l’étude
- La possibilité de vous retirer de l’étude à tout moment
- La couverture assurantielle en cas de dommages liés à l’essai
- L’impact potentiel sur vos autres traitements ou suivis médicaux
La HAS recommande de discuter ouvertement de ces aspects avec l’équipe de recherche, mais aussi avec votre médecin traitant qui connaît votre historique médical complet.
Processus de participation
Le parcours d’un volontaire dans un essai clinique suit une procédure bien définie, destinée à garantir sa sécurité et son consentement éclairé. Comprendre ce processus est essentiel pour toute personne envisageant une participation.
Critères d’éligibilité
Chaque essai clinique définit des critères précis pour sélectionner les participants :
- Critères d’inclusion : caractéristiques requises pour participer (âge, sexe, type et stade de la maladie, antécédents médicaux, etc.)
- Critères d’exclusion : facteurs qui empêchent la participation (certaines comorbidités, grossesse, traitements concomitants incompatibles, etc.)
Ces critères sont établis pour plusieurs raisons :
- Assurer la sécurité des participants
- Cibler les personnes les plus susceptibles de bénéficier du traitement
- Obtenir des résultats scientifiquement valides et interprétables
- Limiter les facteurs pouvant interférer avec l’évaluation du traitement
L’évaluation de l’éligibilité comprend généralement un examen médical complet, des analyses biologiques et parfois des examens d’imagerie. Cette phase de présélection peut prendre plusieurs jours voire semaines selon la complexité de l’essai.
Étapes de l’inscription
Le processus d’inscription à un essai clinique comprend plusieurs étapes importantes :
- Information initiale : première prise de contact avec l’équipe de recherche, présentation générale de l’étude
- Processus de consentement éclairé :
- Présentation détaillée de l’étude (objectifs, déroulement, bénéfices attendus, risques potentiels)
- Remise d’un document d’information complet
- Temps de réflexion obligatoire (généralement plusieurs jours)
- Possibilité de poser toutes les questions nécessaires
- Signature du formulaire de consentement
- Évaluation médicale complète : vérification de l’état de santé et de la compatibilité avec l’essai
- Randomisation : dans les essais comparatifs, attribution aléatoire à un groupe de traitement
- Début du traitement et du suivi selon le protocole établi
Le consentement éclairé est un processus continu : le participant peut à tout moment poser des questions supplémentaires ou se retirer de l’étude sans avoir à se justifier et sans que cela n’affecte la qualité de ses soins ultérieurs.
Parcours du volontaire
Une fois inscrit, le participant suit généralement ce parcours :
- Phase d’inclusion : début officiel de la participation après validation de tous les critères
- Administration du traitement : selon le protocole (dose, fréquence, voie d’administration)
- Visites de suivi : examens réguliers pour évaluer l’efficacité et la tolérance
- Surveillance des effets indésirables : signalement et prise en charge rapide si nécessaire
- Recueil de données : mesures biologiques, questionnaires, examens cliniques
- Fin de participation : soit à la fin prévue de l’essai, soit en cas d’arrêt prématuré
- Suivi post-essai : surveillance prolongée dans certains cas pour détecter d’éventuels effets à long terme
La durée totale de participation varie considérablement selon les essais, de quelques semaines à plusieurs années pour les études de phase IV ou les suivis à long terme.
FAQ sur les essais cliniques
Comment participer à un essai clinique ?
Pour participer à un essai clinique, vous pouvez consulter le registre national des essais cliniques sur le site de l’ANSM, discuter avec votre médecin traitant ou spécialiste qui pourra vous orienter, ou contacter directement les centres de recherche clinique des CHU. Des sites comme ClinicalTrials.gov répertorient également les essais en cours dans le monde entier, avec des critères de recherche par maladie et localisation.
Quels sont les risques d’un essai clinique ?
Les risques incluent des effets secondaires connus ou inconnus du traitement étudié, la possibilité que le traitement soit inefficace ou moins efficace que les alternatives existantes, et les contraintes pratiques (déplacements fréquents, examens nombreux). Le niveau de risque varie selon la phase de l’essai, les essais de phase I comportant généralement plus d’incertitudes que les essais de phases ultérieures.
Puis-je quitter un essai clinique en cours ?
Oui, vous pouvez quitter un essai clinique à tout moment, sans avoir à vous justifier et sans que cela n’affecte la qualité de vos soins ultérieurs. Le consentement éclairé est révocable à tout instant. Il est recommandé d’informer l’équipe de recherche de votre décision pour qu’elle puisse organiser une visite de fin d’étude et assurer la continuité de vos soins.
Les essais cliniques sont-ils rémunérés ?
La situation varie selon le type d’essai. Pour les volontaires sains (essais de phase I principalement), une indemnisation compensatoire est généralement prévue, plafonnée à 4 500€ par an en France. Pour les patients, les essais ne sont généralement pas rémunérés, mais les frais liés à l’étude (déplacements, hébergement) sont pris en charge. Certains essais proposent des dédommagements pour les contraintes subies.
Que se passe-t-il après la fin de l’essai ?
Après la fin de l’essai, le participant retrouve son parcours de soins habituel. Dans certains cas, si le traitement s’est avéré efficace, un accès prolongé ou compassionnel peut être envisagé. Les résultats globaux de l’étude sont généralement communiqués aux participants après analyse complète, ce qui peut prendre plusieurs mois. Un suivi médical post-essai peut être proposé pour surveiller d’éventuels effets à long terme.
Conclusion
Les essais cliniques représentent un pilier fondamental de l’avancée médicale, permettant le développement de nouveaux traitements et l’amélioration des stratégies thérapeutiques existantes. Pour les participants, ils constituent une démarche qui mérite réflexion, mêlant considérations personnelles et contribution à l’intérêt collectif.
La décision de participer à un essai clinique doit résulter d’un choix éclairé, fondé sur une compréhension approfondie des avantages potentiels (accès à des traitements innovants, suivi médical renforcé) et des risques associés (effets secondaires, incertitudes thérapeutiques). Le cadre légal et éthique entourant ces essais offre des garanties importantes, mais ne supprime pas la nécessité d’une évaluation personnelle soigneuse.
Il est recommandé de discuter de cette option avec vos médecins habituels, de poser toutes vos questions à l’équipe de recherche et de prendre le temps de la réflexion avant de vous engager. La participation reste entièrement volontaire et révocable à tout moment.
Pour obtenir des informations complémentaires ou être orienté vers des spécialistes qui pourront vous conseiller sur les essais cliniques dans votre domaine pathologique.